식약처, 전성분 표시 도입‧글자 폰트 크기도 확대
보존제‧타르색소는 성분표시 맨 앞에 표기해야
[caption id="attachment_383112" align="alignleft" width="300"]

지난 5일 서울 코엑스에서 열린 ‘의약품 허가·심사 종합 민원 설명회’에서 정현호 식약처 사무관이 발표하고 있다.[/caption]
[한의신문=최성훈 기자]식품의약품안전처(처장 손문기)는 오는 12월부터 시행되는 ‘의약품 표시 등에 관한 규정’ 개정안에 대해 “소비자가 일반의약품 정보를 보다 알기 쉽도록 하는 게 이번 표준서식의 도입 취지”라고 밝혔다.
정현호 식약처 의약품관리과 사무관은 지난 5일 서울 코엑스에서 열린 ‘의약품 허가·심사 종합 민원 설명회’에서 표준서식 도입 등 개정안의 주요내용을 설명하며 이 같이 말했다.
정 사무관에 따르면 이번 개정안은 소비자들이 의약품 표시 정보를 더욱 쉽게 알 수 있도록 일반의약품의 ‘주표시면’과 ‘정보표시면’으로 구분해 기재하고, 의약품 전성분 표시방법이 신설됐다.
소비자들이 제품에 표시된 △효능·효과 △용법·용량 △사용상의 주의사항 등 정보를 정확하게 확인하고 의약품을 안전하고 올바르게 복용할 수 있도록 지원하기 위해 지난해 12월 국회를 통과됐다.
가장 큰 변화는 일반의약품 외부 용기·포장의 정보표시면에 표준서식 도안을 도입해 ‘규격화’했다. 그 동안 일반의약품 제품 뒷면이나 용기에 나온 정보표시면을 살펴보면 제조회사마다 모양이 제각각이었다. 그러나 이를 규격화해 어떤 일반의약품을 구매하더라도 소비자가 의약품 정보를 보다 알기 쉽도록 직관적으로 바꾼 것이다.
정 사무관은 “표준서식을 어떻게 하면 최적화할 수 있을지 학계와 제약업계, 소비자단체가 지난 1년간 공동 연구를 했다”고 말했다.
도안을 살펴보면 주표시면은 '일반의약품'이라는 문자, 허가 받은 자 또는 수입자 상호, 제품명, 중량 또는 용량이나 개수를 표시한다.
[caption id="attachment_383113" align="alignnone" width="1024"]
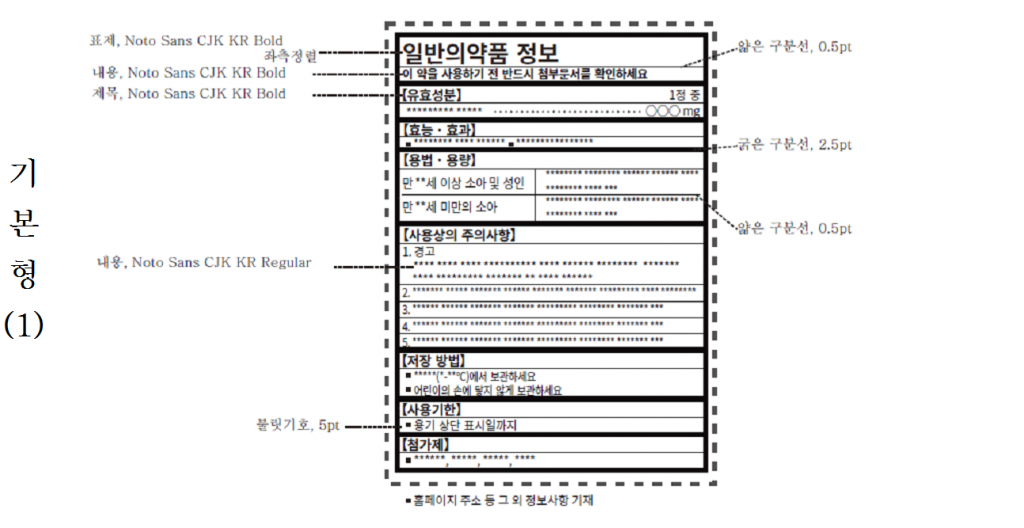
식품의약품안전처가 제시한 의약품 표시 정보 표준서식 도안[/caption]
정보표시면은 원칙적으로 배경은 흰색, 글자는 검은색으로 기재하고 표제는 14포인트, 제목은 8포인트, 내용은 7포인트로 작성하며, 제목과 내용 사이는 0.5포인트의 얇은 선으로 구분해 표시한다.
그는 “아세트아미노펜의 경우 미 FDA의 승인을 받은 소염진통제지만 두통, 생리통 등에 다양하게 활용되다 보니 다른 성분의 소염진통제와 중복복용 하는 사례가 많다”며 “따라서 유효성분이나 경고항을 노란배경으로 강조해 표시할 수도 있다”고 설명했다.
이와 함께 개정안에는 의약품에 포함된 모든 성분을 정보표시면에 기재토록 했다.
정 사무관은 “표시방법은 의약품에 함유된 유효성분, 첨가제 순서로 구분해 기재하게 된다. 첨가제 중 소비자 관심이 높은 보존제나 타르색소 등을 맨 앞에 기재하게 되고 그 외 첨가제를 한글 오름차순으로 표시한다”고 말했다.
이 밖에도 소비자에게 제공되는 첨부 문서의 경우 글자 크기는 9포인트 이상이 권장된다. 외부 용기·포장 면적이 ‘정보표시면’보다 넓은 경우 글자 크기를 더 크게 표시하는 것을 제시했다고 정 사무관은 설명했다.
식약처는 앞서 지난달 20일 ‘의약품 표시 등에 관한 규정’ 행정예고를 하면서 “소비자에게는 의약품 정보를 쉽게 전달해 알 권리를 강화하고, 제약사에게는 의약품 표시에 대한 명확한 기준을 제시해 새로운 제도가 안정적으로 운영되는데 도움이 될 것”이라고 밝혔다.
 속초9.0℃
속초9.0℃ 13.0℃
13.0℃ 철원12.5℃
철원12.5℃ 동두천14.3℃
동두천14.3℃ 파주15.3℃
파주15.3℃ 대관령6.5℃
대관령6.5℃ 춘천13.3℃
춘천13.3℃ 백령도12.8℃
백령도12.8℃ 북강릉9.5℃
북강릉9.5℃ 강릉10.8℃
강릉10.8℃ 동해12.9℃
동해12.9℃ 서울16.0℃
서울16.0℃ 인천14.3℃
인천14.3℃ 원주15.4℃
원주15.4℃ 울릉도14.4℃
울릉도14.4℃ 수원14.8℃
수원14.8℃ 영월15.4℃
영월15.4℃ 충주16.5℃
충주16.5℃ 서산14.6℃
서산14.6℃ 울진14.2℃
울진14.2℃ 청주17.2℃
청주17.2℃ 대전18.8℃
대전18.8℃ 추풍령18.2℃
추풍령18.2℃ 안동19.2℃
안동19.2℃ 상주20.0℃
상주20.0℃ 포항18.9℃
포항18.9℃ 군산14.2℃
군산14.2℃ 대구21.3℃
대구21.3℃ 전주16.0℃
전주16.0℃ 울산22.6℃
울산22.6℃ 창원22.1℃
창원22.1℃ 광주16.1℃
광주16.1℃ 부산20.7℃
부산20.7℃ 통영20.5℃
통영20.5℃ 목포13.3℃
목포13.3℃ 여수19.5℃
여수19.5℃ 흑산도12.7℃
흑산도12.7℃ 완도15.9℃
완도15.9℃ 고창12.8℃
고창12.8℃ 순천17.6℃
순천17.6℃ 홍성(예)16.0℃
홍성(예)16.0℃ 16.6℃
16.6℃ 제주15.2℃
제주15.2℃ 고산12.7℃
고산12.7℃ 성산15.2℃
성산15.2℃ 서귀포18.2℃
서귀포18.2℃ 진주20.3℃
진주20.3℃ 강화15.1℃
강화15.1℃ 양평17.1℃
양평17.1℃ 이천15.7℃
이천15.7℃ 인제9.9℃
인제9.9℃ 홍천15.3℃
홍천15.3℃ 태백14.9℃
태백14.9℃ 정선군13.8℃
정선군13.8℃ 제천13.9℃
제천13.9℃ 보은17.9℃
보은17.9℃ 천안15.7℃
천안15.7℃ 보령16.3℃
보령16.3℃ 부여17.0℃
부여17.0℃ 금산17.8℃
금산17.8℃ 18.0℃
18.0℃ 부안13.7℃
부안13.7℃ 임실14.1℃
임실14.1℃ 정읍14.0℃
정읍14.0℃ 남원16.6℃
남원16.6℃ 장수14.5℃
장수14.5℃ 고창군13.8℃
고창군13.8℃ 영광군12.9℃
영광군12.9℃ 김해시22.5℃
김해시22.5℃ 순창군15.4℃
순창군15.4℃ 북창원22.4℃
북창원22.4℃ 양산시23.7℃
양산시23.7℃ 보성군17.0℃
보성군17.0℃ 강진군16.2℃
강진군16.2℃ 장흥16.9℃
장흥16.9℃ 해남14.4℃
해남14.4℃ 고흥17.8℃
고흥17.8℃ 의령군20.4℃
의령군20.4℃ 함양군19.0℃
함양군19.0℃ 광양시19.5℃
광양시19.5℃ 진도군13.5℃
진도군13.5℃ 봉화17.2℃
봉화17.2℃ 영주16.5℃
영주16.5℃ 문경18.4℃
문경18.4℃ 청송군19.6℃
청송군19.6℃ 영덕16.0℃
영덕16.0℃ 의성20.7℃
의성20.7℃ 구미20.9℃
구미20.9℃ 영천20.9℃
영천20.9℃ 경주시22.9℃
경주시22.9℃ 거창20.9℃
거창20.9℃ 합천21.4℃
합천21.4℃ 밀양23.1℃
밀양23.1℃ 산청18.7℃
산청18.7℃ 거제19.9℃
거제19.9℃ 남해19.3℃
남해19.3℃ 23.2℃
23.2℃









![[자막뉴스] 서울시 한의약 치매 건강증진사업, 어르신 건강 증진에 한 몫](https://www.akomnews.com/data/photo/2512/990852453_gWjQvmYX_208ec3d22cca3c4dabe0690736cb02fecca2d1b0.jpg)
![[자막뉴스] 국회와 정부, K-MEDI 동행 선언](https://www.akomnews.com/data/photo/2512/990852453_pWMfBulG_1f19604ef50b802d08e2eba88760392f36a0c023.jpg)
![[자막뉴스] '2025 한의혜민대상' 원성호 서울대 보건대학교 교수 대상](https://www.akomnews.com/data/photo/2512/990852453_9aoWOQ7J_f562bba0ac6cd1fa3cb3e0cfa693448832494455.jpg)


![[여한의사회] "세계가 주목하는 침술의 힘"](https://www.akomnews.com/data/photo/2507/2039300137_tzacLJfB_2f59361a10063749b72d0e25ccb1a8ab9fe13f47.jpg)






















