[한의신문=김대영 기자]식품의약품안전처(처장 이의경, 이하 식약처)가 25일 ‘모바일 의료용 앱 안전관리 지침’을 개정‧발간했다.
식약처는 ‘모바일 의료용 앱’이 의료기기로 허가를 받게 되면 스마트워치, 스마트폰과 같이 해당 앱과 연동되는 모바일 플랫폼은 허가를 받을 필요가 없게 돼 의료제품의 시장진입 시기가 단축되고 소비자들이 자신의 건강상태를 정확한 데이터로 상시 확인할 수 있게 될 것으로 기대했다.
'모바일 의료용 앱 안전관리 지침' 주요 개정 내용은 △모바일 의료용 앱 형태별 예시 및 허가방안 △이미 판매된 모바일 플랫폼에 설치(판매)가능 △상용모바일 플랫폼 허가대상 제외 △모바일 의료용 앱 품질관리 운영요령 등이다.
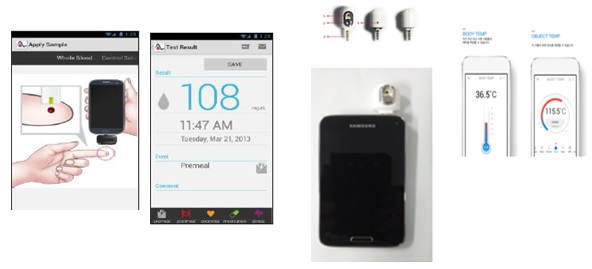
모바일 의료용 앱 허가관리 대상은 △의료기기를 무선으로 제어하는 모바일 앱 △질병의 진단 또는 환자 모니터링 등을 위해 의료기기에서 측정된 데이터 등을 받아 표시 또는 분석하는 모바일 앱 △모바일 플랫폼에 별도의 전극, 프로브 등이 연결되어 의료기기로 동작할 수 있도록 하는 모바일 앱 △모바일 플랫폼에 내장된 센서 등을 이용하여 의료기기로 사용하는 모바일 앱 △환자에 대한 분석․질병 진단 또는 치료법을 제공하는 모바일 앱이다.
구체적으로 살펴보면 의료기기를 무선으로 제어하는 모바일 앱은 의료기기와 연동돼 무선으로 의료기기를 제어하는 모바일 앱으로 특정 의료기기의 부분품에 해당된다.
예를 들어 인슐린 펌프로 신호를 전송해 인슐린 분비를 제어하는 모바일 앱이나 혈압계의 커프 압력을 제어하는 모바일 앱, CT나 X- Ray 촬영 시 기기를 제어하는 모바일 앱, 이식형근육․신경자극기를 세팅하고 제어하는 모바일 앱, 임플란트 달팽이관을 세팅하고 제어하는 모바일 앱과 같이 무선으로 제어되는 의료기기를 제어하기 위해 모바일 플랫폼에 설치해 사용하는 모바일 앱이 여기에 해당한다.
이러한 모바일 의료용 앱은 특정 의료기기 허가 신청서에 함께 기재돼 심사 후 허가된다.
또 질병의 진단 또는 환자 모니터링 등을 위해 의료기기에서 측정된 각종 데이터, 촬영된 의료영상 등을 전송받아 진단하거나 환자 모니터링 등 의료 목적으로 표시‧분석하는 모바일 앱은 의료기기에 해당한다.
특정 의료기기의 구성품으로 제조돼 사용되는 모바일 앱은 함께 사용하는 의료기기의 부분품에 해당해 특정 의료기기와 함께 심사해 허가될 수 있으나, 특정한 의료기기를 정하지 않고 통신환경, 운영체제 등이 호환돼 범용으로 사용될 수 있거나 원격으로 환자의 영상 또는 데이터를 전송하는 앱 등은 그 자체가 의료기기에 해당해 단독으로 심사돼 허가될 수 있다.
환자 모니터링 목적의 모바일 앱, 태아의 심장 박동 데이터와 자궁 수축정도를 전송받아 분만 과정 모니터링이 가능 하도록 표시하는 모바일 앱, 의료영상저장전송장치에서 전송 받은 의료영상을 확대‧ 축소‧ 조회하는 모바일 앱, 혈당측정기‧혈압계 등에서 측정된 값을 전송받아 분석하는 모바일 앱, 혈당측정기‧혈압계 등의 의료기기에서 측정된 데이터를 전송받아 원격의료 등을 위해 서버로 전송하는 모바일 앱 등이 여기에 해당된다.
모바일 플랫폼에 별도의 전극, 프로브, 센서 등(이하 전극 등)을 연결해 의료기기로 사용할 수 있도록 하는 기능을 갖는 모바일 앱 또한 의료기기에 해당한다.
이에 해당하는 모바일 의료용 앱은 전극 등과 함께 구성돼 사용하도록 제조된 것으로 허가 시 함께 사용하는 전극 등과 같이 심사 후 허가된다.
다만 특정한 전극 등이 정해지지 않고 기 허가된 전극 등을 사용할 수 있으며 이 경우 사용가능한 전극 등을 허가신청서에 기재하고 시험검사 등을 통해 안전성․유효성에 대한 자료를 제출․입증하는 경우에는 모바일 의료용 앱 단독으로 심사 후 허가 될 수 있다.
혈당측정기가 연결되어 혈당 값을 측정하고 표시하는 모바일 앱, 모바일 플랫폼에 센서를 연결해 심장 등 내부기관과 연관된 소리를 듣기 위해 전기적으로 증폭시키는 모바일 앱, 모바일 플랫폼에 센서를 연결해 특정 질병의 원인이 되는 떨림 정도를 측정하는 모바일 앱, 진단 등 의료 목적으로 모바일 플랫폼에 센서를 연결해 혈액 내 산소포화도를 측정하는 모바일 앱 등이 해당된다.
모바일 플랫폼에 내장(또는 별도로 추가된)된 센서 등을 이용해 모바일 플랫폼을 의료기기로 사용하는 모바일 앱도 의료기기에 해당된다.
예를 들어 모바일 플랫폼의 광원, 마이크 등과 같이 기본으로 내장된 센서 또는 의료기기 성능을 구현하기 위해 별도로 장착된 센서 등을 이용해 질병 진단 등을 목적으로 혈류량, 산소포화도, 심전도 등을 측정․분석하는 모바일 앱이 이에 해당한다.
이 경우 모바일 플랫폼에서 측정되는 신호의 정확성, 인체 접촉시 안전성 등 의료기기 안전성․유효성은 관련 국내외 기준규격에 따른 시험검사 등 기술문서 심사 등에 관한 자료를 제출해 심사하되 허가신청서에는 모바일 앱만을 기재해 허가될 수 있다.
환자에 대한 분석․질병 진단 또는 치료법을 제공하는 모바일 앱은 의료기기에서 나온 데이터를 입력하거나 전송받아 환자 특이적 분석을 수행하는 모바일 앱 또는 데이터를 해석해 진단 또는 치료법을 제공하는 모바일 앱을 말한다.
예를 들면 유전자검사 결과를 입력해 분석하고 환자의 특정 암 발병확률, 병기 등을 진단하는 모바일 앱이나 조직검사 결과 등 병리검사 또는 진단검사 결과를 입력해 암 발병 확률, 전이 확률, 병기 등을 분석‧진단하는 모바일 앱, 질병의 예방, 처치 또는 치료 목적으로 사용되는 모바일 앱(소프트웨어 프로그램)으로 독립적으로 사용될 수도 있고, 치료효과를 높이기 위해 다른 의약품이나 의료기기와 함께 사용될 수 있는 디지털 치료기기(Digital Therapeutics) 등이 여기에 해당한다.
이 경우 모바일 의료용 앱이 단독으로 의료기기적 성능을 발휘하는 것으로 모바일 의료용 앱 단독으로 심사 후 허가될 수 있다.
식약처는 이번 지침 발간으로 디지털 헬스케어 기업들이 의료기술과 소프트웨어를 접목하는 모바일 의료용 앱을 개발하고 제품화하는데 도움이 될 것으로 기대하며 우리나라의 모바일 기기 및 소프트웨어 기술이 접목된 의료기기가 세계시장에 신속히 진출할 수 있도록 관련 제도를 적극적으로 개선해 나간다는 방침이다.
 속초5.9℃
속초5.9℃ -6.3℃
-6.3℃ 철원-8.0℃
철원-8.0℃ 동두천-3.3℃
동두천-3.3℃ 파주-5.0℃
파주-5.0℃ 대관령-2.4℃
대관령-2.4℃ 춘천-5.1℃
춘천-5.1℃ 백령도8.6℃
백령도8.6℃ 북강릉1.7℃
북강릉1.7℃ 강릉4.0℃
강릉4.0℃ 동해1.4℃
동해1.4℃ 서울-0.7℃
서울-0.7℃ 인천0.8℃
인천0.8℃ 원주-5.0℃
원주-5.0℃ 울릉도4.1℃
울릉도4.1℃ 수원-2.8℃
수원-2.8℃ 영월-7.5℃
영월-7.5℃ 충주-7.1℃
충주-7.1℃ 서산2.8℃
서산2.8℃ 울진0.5℃
울진0.5℃ 청주-3.5℃
청주-3.5℃ 대전-5.3℃
대전-5.3℃ 추풍령-7.9℃
추풍령-7.9℃ 안동-8.3℃
안동-8.3℃ 상주-4.0℃
상주-4.0℃ 포항0.2℃
포항0.2℃ 군산-4.0℃
군산-4.0℃ 대구-4.1℃
대구-4.1℃ 전주-3.9℃
전주-3.9℃ 울산-0.8℃
울산-0.8℃ 창원-1.3℃
창원-1.3℃ 광주-3.0℃
광주-3.0℃ 부산0.9℃
부산0.9℃ 통영-0.4℃
통영-0.4℃ 목포-1.5℃
목포-1.5℃ 여수-0.2℃
여수-0.2℃ 흑산도4.8℃
흑산도4.8℃ 완도-2.1℃
완도-2.1℃ 고창-6.3℃
고창-6.3℃ 순천-8.5℃
순천-8.5℃ 홍성(예)0.2℃
홍성(예)0.2℃ -6.0℃
-6.0℃ 제주5.3℃
제주5.3℃ 고산6.0℃
고산6.0℃ 성산4.1℃
성산4.1℃ 서귀포5.6℃
서귀포5.6℃ 진주-7.3℃
진주-7.3℃ 강화-0.5℃
강화-0.5℃ 양평-3.5℃
양평-3.5℃ 이천-6.0℃
이천-6.0℃ 인제-5.5℃
인제-5.5℃ 홍천-4.5℃
홍천-4.5℃ 태백-5.8℃
태백-5.8℃ 정선군-10.1℃
정선군-10.1℃ 제천-6.8℃
제천-6.8℃ 보은-8.1℃
보은-8.1℃ 천안-5.9℃
천안-5.9℃ 보령3.1℃
보령3.1℃ 부여-5.0℃
부여-5.0℃ 금산-7.9℃
금산-7.9℃ -5.2℃
-5.2℃ 부안-3.5℃
부안-3.5℃ 임실-8.1℃
임실-8.1℃ 정읍-5.3℃
정읍-5.3℃ 남원-7.7℃
남원-7.7℃ 장수-9.5℃
장수-9.5℃ 고창군-5.3℃
고창군-5.3℃ 영광군-5.5℃
영광군-5.5℃ 김해시-2.0℃
김해시-2.0℃ 순창군-7.2℃
순창군-7.2℃ 북창원-2.2℃
북창원-2.2℃ 양산시-1.0℃
양산시-1.0℃ 보성군-4.7℃
보성군-4.7℃ 강진군-6.0℃
강진군-6.0℃ 장흥-7.9℃
장흥-7.9℃ 해남-7.0℃
해남-7.0℃ 고흥-7.6℃
고흥-7.6℃ 의령군-9.3℃
의령군-9.3℃ 함양군-9.1℃
함양군-9.1℃ 광양시-2.6℃
광양시-2.6℃ 진도군-3.5℃
진도군-3.5℃ 봉화-11.3℃
봉화-11.3℃ 영주-8.6℃
영주-8.6℃ 문경-6.1℃
문경-6.1℃ 청송군-11.1℃
청송군-11.1℃ 영덕0.2℃
영덕0.2℃ 의성-9.6℃
의성-9.6℃ 구미-6.3℃
구미-6.3℃ 영천-7.0℃
영천-7.0℃ 경주시-5.4℃
경주시-5.4℃ 거창-10.2℃
거창-10.2℃ 합천-7.4℃
합천-7.4℃ 밀양-6.8℃
밀양-6.8℃ 산청-8.2℃
산청-8.2℃ 거제-2.2℃
거제-2.2℃ 남해-1.4℃
남해-1.4℃ -6.1℃
-6.1℃






![[자막뉴스] 원외탕전실 평가인증 기준안 공개](https://www.akomnews.com/data/photo/2511/990852453_sZe8qrSG_7e230c1cbeebc4cbde8cec6a32ca9706a4284105.jpg)
![[자막뉴스] 한의사의 레이저 국소마취제 활용은 '합법'](https://www.akomnews.com/data/photo/2511/990852453_sfab7vrl_33eba149666249edcd87064b2ed4efb96506b17f.jpg)
![[자막뉴스] 각 지역 특성 살려 한의약 육성 계획 추진](https://www.akomnews.com/data/photo/2511/990852453_I1rBAk7d_f3b06ec77f325427a6cdd35aad05812b1d2554e2.jpg)
![[자막뉴스] 한의진료 보장 시 5세대 실손보험으로 전환](https://www.akomnews.com/data/photo/2511/990852453_YuT9QS6A_aa357fc96d70718865b613b105f5857705194083.jpg)
![[여한의사회] "세계가 주목하는 침술의 힘"](https://www.akomnews.com/data/photo/2507/2039300137_tzacLJfB_2f59361a10063749b72d0e25ccb1a8ab9fe13f47.jpg)

























